Mga bagong publikasyon
Ang closed-loop na sistema ng paghahatid ng gamot ay maaaring mapabuti ang paggamot sa chemotherapy
Huling nasuri: 02.07.2025

Ang lahat ng nilalaman ng iLive ay medikal na nasuri o naka-check ang katotohanan upang masiguro ang mas tumpak na katumpakan hangga't maaari.
Mayroon kaming mahigpit na mga panuntunan sa pag-uukulan at nag-uugnay lamang sa mga kagalang-galang na mga site ng media, mga institusyong pang-akademikong pananaliksik at, hangga't maaari, ang mga pag-aaral ng medikal na pag-aaral. Tandaan na ang mga numero sa panaklong ([1], [2], atbp) ay maaaring i-click na mga link sa mga pag-aaral na ito.
Kung sa tingin mo na ang alinman sa aming nilalaman ay hindi tumpak, hindi napapanahon, o kung hindi pinag-uusapan, mangyaring piliin ito at pindutin ang Ctrl + Enter.
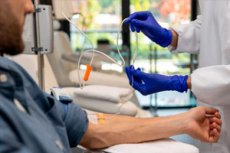
Kapag ang mga pasyente ng kanser ay sumasailalim sa chemotherapy, ang mga dosis ng karamihan sa mga gamot ay kinakalkula batay sa ibabaw ng katawan ng pasyente. Ito ay tinatantya gamit ang isang equation na isinasaalang-alang ang taas at timbang ng pasyente. Ang equation na ito ay nabuo noong 1916 batay sa data mula sa siyam na pasyente lamang.
Ang pinasimpleng diskarte sa dosing na ito ay hindi isinasaalang-alang ang iba pang mga kadahilanan at maaaring magresulta sa isang pasyente na mabigyan ng sobra o masyadong maliit na gamot. Bilang resulta, ang ilang mga pasyente ay maaaring makaranas ng hindi kinakailangang toxicity o hindi sapat na bisa mula sa chemotherapy na kanilang natatanggap.
Upang mapabuti ang katumpakan ng dosing ng chemotherapy, ang mga inhinyero ng MIT ay bumuo ng isang alternatibong diskarte na nagpapahintulot sa dosis na ma-personalize para sa bawat pasyente. Sinusukat ng kanilang system ang dami ng gamot sa katawan ng pasyente at pinapakain ang data na iyon sa isang controller na maaaring ayusin ang rate ng pagbubuhos nang naaayon.
Ang diskarte na ito ay maaaring makatulong na mabayaran ang mga pagkakaiba sa mga pharmacokinetics ng gamot na dulot ng komposisyon ng katawan, genetic predisposition, chemotherapy-induced organ toxicity, mga pakikipag-ugnayan sa iba pang mga gamot at pagkain, at mga circadian variation sa mga enzyme na responsable sa pagbagsak ng mga chemotherapy na gamot, sabi ng mga mananaliksik.
"Sa pamamagitan ng pagkilala sa mga pagsulong sa pag-unawa kung paano na-metabolize ang mga gamot at paglalapat ng mga tool sa engineering upang pasimplehin ang personalized na dosing, naniniwala kaming makakatulong kami sa pagbabago ng kaligtasan at pagiging epektibo ng maraming gamot," sabi ni Giovanni Traverso, isang associate professor ng mechanical engineering sa MIT, isang gastroenterologist sa Brigham and Women's Hospital, at senior author ng pag-aaral.
Si Louis DeRidder, isang nagtapos na mag-aaral sa MIT, ay ang nangungunang may-akda ng papel na inilathala sa journal Med.
Patuloy na pagsubaybay
Sa pag-aaral na ito, ang mga mananaliksik ay nakatuon sa isang gamot na tinatawag na 5-fluorouracil, na ginagamit upang gamutin ang colorectal cancer at iba pang mga kanser. Ang gamot ay karaniwang ibinibigay sa loob ng 46 na oras, at ang dosis nito ay tinutukoy gamit ang isang formula batay sa taas at timbang ng pasyente, na nagbibigay ng isang pagtatantya ng ibabaw ng katawan.
Gayunpaman, hindi isinasaalang-alang ng diskarteng ito ang mga pagkakaiba sa komposisyon ng katawan na maaaring makaapekto sa kung paano ipinamamahagi ang gamot sa katawan, o mga pagkakaiba-iba ng genetic na nakakaapekto sa kung paano ito na-metabolize. Ang mga pagkakaibang ito ay maaaring humantong sa mga mapaminsalang epekto kung labis ang gamot na ibinigay. Kung hindi sapat ang ibinigay na gamot, maaaring hindi nito mapatay ang tumor gaya ng inaasahan.
"Ang mga taong may parehong lugar sa ibabaw ng katawan ay maaaring magkaroon ng iba't ibang taas at timbang, iba't ibang mass ng kalamnan, o iba't ibang genetika, ngunit hangga't ang taas at bigat na naka-plug sa equation na iyon ay nagbubunga ng parehong lugar sa ibabaw ng katawan, ang kanilang dosis ay magkapareho," sabi ni DeRidder, isang PhD na kandidato sa medical engineering at medical physics program sa Harvard-MIT Program sa Health Sciences and Technology.
Ang isa pang salik na maaaring magbago sa dami ng gamot sa dugo sa anumang oras ay ang circadian variation sa isang enzyme na tinatawag na dihydropyrimidine dehydrogenase (DPD), na sumisira sa 5-fluorouracil. Ang pagpapahayag ng DPD, tulad ng maraming iba pang mga enzyme sa katawan, ay kinokontrol ng isang circadian ritmo. Kaya, ang pagkasira ng 5-FU ng DPD ay hindi pare-pareho, ngunit nag-iiba sa oras ng araw. Ang mga circadian rhythm na ito ay maaaring magresulta sa sampung beses na pagkakaiba-iba sa dami ng 5-FU sa dugo ng isang pasyente sa panahon ng pagbubuhos.
"Sa pamamagitan ng paggamit ng body surface area upang kalkulahin ang dosis ng chemotherapy, alam namin na ang dalawang tao ay maaaring magkaroon ng magkaibang mga toxicity mula sa 5-fluorouracil. Ang isang pasyente ay maaaring magkaroon ng mga cycle ng paggamot na may kaunting toxicity, at pagkatapos ay isang cycle na may kahila-hilakbot na toxicity. May nagbago sa paraan ng pag-metabolize ng pasyente ng chemotherapy mula sa isang cycle patungo sa susunod. Ang aming lumang paraan ng dosing ay hindi nakakakuha ng mga pagbabagong ito, at sinabi ng mga pasyente na si Douglas o Runcologist ay hindi nagdurusa sa mga pagbabagong ito, at sinabi ng mga pasyente ng isang Runcologist, at ang mga pasyente ay hindi nakakakuha ng mga pagbabagong ito, at sinabi ng isang Runcologist na si Douglas. Dana-Farber Cancer Institute at isang may-akda ng papel.
Ang isang paraan upang subukang mabayaran ang pagkakaiba-iba sa mga pharmacokinetics ng chemotherapy ay isang diskarte na tinatawag na therapeutic drug monitoring, kung saan ang pasyente ay nagbibigay ng sample ng dugo sa pagtatapos ng isang ikot ng paggamot. Matapos masuri ang sample na ito para sa mga konsentrasyon ng gamot, ang dosis ay maaaring iakma, kung kinakailangan, sa simula ng susunod na cycle (karaniwan ay dalawang linggo para sa 5-fluorouracil).
Ang diskarte na ito ay ipinakita na humantong sa mas mahusay na mga kinalabasan para sa mga pasyente, ngunit hindi malawakang ginagamit para sa mga chemotherapies tulad ng 5-fluorouracil.
Nais ng mga mananaliksik ng MIT na bumuo ng isang katulad na uri ng pagsubaybay, ngunit sa isang automated na paraan na magpapahintulot sa dosing ng gamot na ma-personalize sa real time, na maaaring humantong sa mas mahusay na mga resulta para sa mga pasyente.
Sa kanilang closed-loop system, ang mga konsentrasyon ng gamot ay maaaring patuloy na masubaybayan at ang impormasyong ito ay ginagamit upang awtomatikong ayusin ang rate ng pagbubuhos ng gamot na chemotherapy upang mapanatili ang dosis sa loob ng target na hanay.
Nagbibigay-daan ang closed-loop system na ito na ma-personalize ang dosing ng gamot upang isaalang-alang ang mga circadian ritmo ng mga antas ng enzyme na nag-metabolize ng gamot, gayundin ang anumang pagbabago sa mga pharmacokinetics ng pasyente mula noong huling paggamot, gaya ng toxicity ng organ na dulot ng chemotherapy.
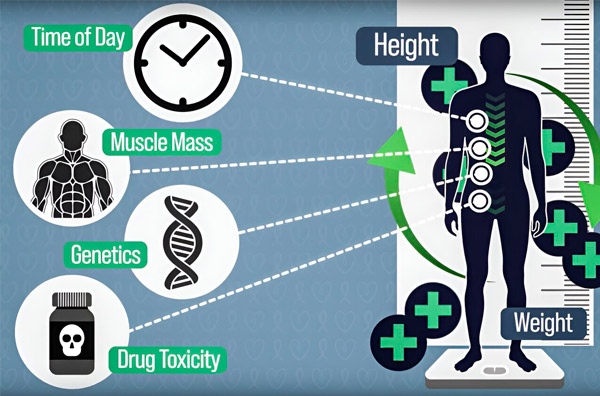
Upang gawing mas tumpak ang dosing ng chemotherapy, gumawa ang mga inhinyero ng MIT ng paraan upang patuloy na sukatin ang dami ng gamot sa katawan ng isang pasyente sa panahon ng multi-hour infusion. Makakatulong ito na mabayaran ang mga pagkakaiba na dulot ng komposisyon ng katawan, genetics, toxicity sa droga, at circadian oscillations. Pinagmulan: Kagandahang-loob ng mga mananaliksik.
Ang bagong sistema na binuo ng mga mananaliksik, na kilala bilang CLAUDIA (Closed-Loop AUtomated Drug Infusion regulAtor), ay gumagamit ng mga kagamitang magagamit sa komersyo para sa bawat hakbang. Kinukuha ang mga sample ng dugo tuwing limang minuto at mabilis na inihanda para sa pagsusuri. Ang konsentrasyon ng 5-fluorouracil sa dugo ay sinusukat at inihambing sa target na hanay.
Ang pagkakaiba sa pagitan ng target at nasusukat na mga konsentrasyon ay ipinasok sa isang control algorithm, na pagkatapos ay inaayos ang rate ng pagbubuhos kung kinakailangan upang mapanatili ang dosis sa loob ng hanay ng mga konsentrasyon kung saan ang gamot ay epektibo at hindi nakakalason.
"Bumuo kami ng isang sistema kung saan maaari naming patuloy na masukat ang konsentrasyon ng gamot at ayusin ang rate ng pagbubuhos nang naaayon upang mapanatili ang konsentrasyon ng gamot sa therapeutic window," sabi ni DeRidder.
Mabilis na pagsasaayos
Sa mga pagsusuri sa hayop, natuklasan ng mga mananaliksik na ang paggamit ng CLAUDIA ay maaari nilang panatilihin ang dami ng gamot na nagpapalipat-lipat sa katawan sa target na hanay ng halos 45 porsiyento ng oras.
Ang mga antas ng gamot sa mga hayop na binigyan ng chemotherapy na walang CLAUDIA ay nanatili sa target na hanay lamang ng 13 porsiyento ng oras sa karaniwan. Hindi sinubukan ng mga mananaliksik ang pagiging epektibo ng mga antas ng gamot sa pag-aaral na ito, ngunit ang pagpapanatili ng mga konsentrasyon sa target na window ay naisip na magreresulta sa mas mahusay na mga resulta at mas kaunting toxicity.
Nagawa rin ni CLAUDIA na mapanatili ang 5-fluorouracil na dosis sa target na hanay kahit na ang isang gamot na pumipigil sa DPD enzyme ay pinangangasiwaan. Sa mga hayop na binigyan ng inhibitor na ito nang walang patuloy na pagsubaybay at pagsasaayos, ang mga antas ng 5-fluorouracil ay tumaas hanggang walong beses.
Para sa pagpapakitang ito, manu-manong isinagawa ng mga mananaliksik ang bawat hakbang ng proseso gamit ang mga kagamitang wala sa istante, ngunit plano ngayon na i-automate ang bawat hakbang upang magawa ang pagsubaybay at pagsasaayos ng dosis nang walang interbensyon ng tao.
Upang sukatin ang mga konsentrasyon ng gamot, ginamit ng mga mananaliksik ang high-performance liquid chromatography-mass spectrometry (HPLC-MS), isang pamamaraan na maaaring iakma upang makita ang halos anumang uri ng gamot.
"Nakikita namin ang isang hinaharap kung saan maaari naming gamitin ang CLAUDIA para sa anumang gamot na may naaangkop na mga katangian ng pharmacokinetic at nakikita ng HPLC-MS, na nagbibigay-daan para sa personalized na dosing para sa maraming iba't ibang mga gamot," sabi ni DeRidder.
