Medikal na dalubhasa ng artikulo
Mga bagong publikasyon
Kasalukuyang pananaw sa mga pathogenetic na mekanismo ng hyperuricemia
Huling nasuri: 07.07.2025

Ang lahat ng nilalaman ng iLive ay medikal na nasuri o naka-check ang katotohanan upang masiguro ang mas tumpak na katumpakan hangga't maaari.
Mayroon kaming mahigpit na mga panuntunan sa pag-uukulan at nag-uugnay lamang sa mga kagalang-galang na mga site ng media, mga institusyong pang-akademikong pananaliksik at, hangga't maaari, ang mga pag-aaral ng medikal na pag-aaral. Tandaan na ang mga numero sa panaklong ([1], [2], atbp) ay maaaring i-click na mga link sa mga pag-aaral na ito.
Kung sa tingin mo na ang alinman sa aming nilalaman ay hindi tumpak, hindi napapanahon, o kung hindi pinag-uusapan, mangyaring piliin ito at pindutin ang Ctrl + Enter.
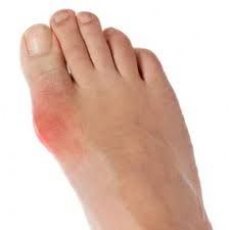
Ang gout ay isang sistematikong sakit na tophaceous na nailalarawan sa pamamagitan ng pagtitiwalag ng sodium monourate crystals sa iba't ibang organo at tissue at ang nagreresultang pamamaga sa mga indibidwal na may hyperuricemia na sanhi ng kapaligiran at/o genetic na mga kadahilanan. Ang pathogenesis ng gout ay batay sa isang disorder ng metabolismo ng uric acid (purine) at isang pagtaas sa nilalaman ng uric acid (UA) sa dugo. Ang batayan ng metabolismo ng uric acid ay ang hyperproduction at pagbaba ng excretion ng mga bato. Kasabay nito, 10% lamang ng mga pasyente na may pangunahing gout ang may mga karamdaman na may lamang endogenous uric acid formation. Sa iba pang mga pasyente, ang pangunahing kadahilanan sa pagbuo ng hyperuricemia ay isang karamdaman sa paglabas ng uric acid ng mga bato.
Bilang karagdagan sa pinsala sa musculoskeletal system, ang gout ay nailalarawan sa pagkakaroon ng visceral manifestations, isa sa mga ito ay urate nephropathy. Ang urate nephropathy ay isang variant ng talamak na tubulointerstitial nephritis, na nailalarawan sa pamamagitan ng akumulasyon ng mga kristal ng uric acid sa interstitium na may pag-unlad ng isang pangalawang nagpapasiklab na proseso sa loob nito at pinsala sa epithelium ng tubular apparatus na may paglabag sa pag-andar nito at mga proseso ng reabsorption.
Ang transportasyon ng uric acid ng mga bato ay isang kaskad ng apat na proseso: glomerular filtration, halos kumpletong reabsorption ng na-filter na uric acid, pagtatago, at postscretory reabsorption sa proximal tubule. Ang urate ay hindi nakagapos sa protina at samakatuwid ay malayang sinasala sa glomeruli. Ang rate ng tubular secretion ay mas mababa kaysa sa rate ng tubular reabsorption, at samakatuwid ang kontribusyon ng secreted urate sa kabuuang halaga ng excreted urate ay maliit. Halos 98-100% ng na-filter na uric acid ay na-reabsorbed sa proximal tubule, pagkatapos kung saan 50% ng na-filter na urate ay na-resecreted, at pagkatapos ay halos 80% ng excreted urate ay na-reabsorbed, at sa huli ay humigit-kumulang 7-10% ng na-filter na urate ay excreted. Ang mga yugto ng reabsorption, pagtatago, at postscretory reabsorption ay nangyayari sa proximal tubule. Ang mga proseso ng reabsorption at pagtatago ay isinasagawa ng mga tiyak na molekula (transporter) na matatagpuan sa hangganan ng brush ng epithelium ng proximal tubules.
Karamihan sa mga urate transporter ay kabilang sa pamilya ng OAT. Ang tubular reabsorption ng urate ay ginagawa ng isang organic anion transporter (urate anion exchanger) na kinilala bilang URAT1 (naka-encode ng SLC22A12 gene). Ang transporter na ito ay naroroon lamang sa mga tao. Maraming mga pag-aaral, kabilang ang mga indibidwal na may familial hyporuricemia, ay nagpapahiwatig ng isang mutation sa SLC22A12 gene na naka-encode sa URAT1 transporter. Napag-alaman na ang mga pasyenteng ito ay halos walang epekto ng probenecid at pyridinamide (isang anti-tuberculosis na gamot na may antiuricosuric effect) sa paglabas ng uric acid.
Bilang karagdagan sa URAT1, mayroong iba pang mga transporter: URATv1, SLC5A8 na naka-encode na sodium-dependent na counter-transporter, mga organic na anion transporter ng pamilyang OAT (OAT1 at OAT3, OAT2 at OAT4), ABCG2 (urate transporter sa pagkolekta ng mga tubules), SLC2A3 (sodium/phosphate counter-transporter ng proximal tubules). Ang OAT2 at OAT4 ay matatagpuan sa apical membrane ng proximal tubules OAT1 at OAT3 sa basolateral na bahagi nito, ang kanilang pangunahing pag-andar ay ang pagpapalitan ng mga organic na anion at bicarboxylate, ngunit sa parehong oras mayroong data sa kanilang epekto sa transportasyon ng urates.
Ang URATv1 (OATv1), na kalaunan ay pinangalanang GLUT9, na na-encode ng SLC2A9 gene, ay isang transporter na umaasa sa boltahe ng mga organikong ion, pangunahin ang glucose at fructose, pati na rin ang isang urate transporter, ang polymorphism ng gene na ito ay nauugnay sa hypouricemia, na nakumpirma sa genetic studies.
Hindi gaanong pinag-aralan ang mga mekanismong nakakaapekto sa pagtatago ng uric acid. Ang kapansanan sa pagtatago ay nauugnay sa mga pagbabago sa bomba na umaasa sa ATP, mga mutasyon sa MRP4 gene na naka-encode sa pagbuo ng uromodulin (Tamm-Horsfall protein, ABSG2 gene). Ang eksaktong mekanismo kung saan ang uromodulin ay nakakaapekto sa pagtatago ng urates ay hindi pa rin alam, marahil ito ay nauugnay sa isang pagtaas sa reabsorption ng sodium sa proximal tubules at uric acid sa parehong oras.
Ang mga may kapansanan sa renal transporter na may mas mataas na uric acid reabsorption ay maaaring humantong sa hyperuricemia at, sa huli, gout. Ang isang bilang ng mga pag-aaral sa urate transporter dysfunction ay nakilala ang genetic mutations, habang ang karamihan sa mga pag-aaral na ito ay nakatuon sa pagkakaroon ng genetic mutations sa urate transporters sa mga pasyente na may hypouricemia, habang ang isyu ng pagkakaroon ng mutations sa mga pasyente na may hyperuricemia ay nananatiling hindi gaanong pinag-aralan. Tandaan ay ang data sa pag-activate ng URAT1 at GLUT9 transporters na may purine-rich diet, arterial hypertension, at lokal na ischemia, na nagiging sanhi ng pagtaas ng uric acid reabsorption. Mayroong katibayan na ang apical tubular reabsorption ng urates at sodium sa pamamagitan ng URAT1 ay may kapansanan, na may kasunod na pag-unlad ng hyperuricemia sa ilalim ng impluwensya ng diabetic ketoacidosis, ethanolamine intoxication, pyrazinamide treatment, hyperinsulinemia, at metabolic syndrome. Kaya, ang kapansanan sa renal uric acid excretion ay maaaring pangalawang proseso dahil sa pinsala sa renal tubular apparatus.
Ang gawain ng tubular apparatus sa mga pasyente na may gota ay maaaring masuri sa pamamagitan ng pang-araw-araw na paglabas, clearance, excreted fraction (EF), reabsorption ng uric acid, calcium (Ca), phosphorus (P), at ammonia excretion. Bukod dito, ang isang "standard" na pagsusuri ng pasyente ay hindi nagpapahintulot sa pagtukoy ng mga palatandaan ng dysfunction ng bato. Ang pinakasimpleng at pinaka-naa-access na paraan ay upang masuri ang clearance ng uric acid na may kasunod na muling pagkalkula sa lugar ng ibabaw ng katawan. Ang aming mga pag-aaral sa mga pasyente na may gota ay nagpakita ng isang medyo mataas na nilalaman ng impormasyon ng pagsusulit na ito para sa pagtukoy ng mga palatandaan ng urate nephropathy, kaya ang halaga ng uric acid clearance na mas mababa sa 7 ml / min / 1.73 m2 ay may sensitivity ng 90% at isang pagtitiyak ng 66%.
Postgraduate na estudyante ng Department of Hospital Therapy Khalfina Tamila Nilovna. Modernong pananaw sa pathogenetic na mekanismo ng hyperuricemia // Practical Medicine. 8 (64) Disyembre 2012 / Volume 1


 [
[