Medikal na dalubhasa ng artikulo
Mga bagong publikasyon
Restenosis
Huling nasuri: 04.07.2025

Ang lahat ng nilalaman ng iLive ay medikal na nasuri o naka-check ang katotohanan upang masiguro ang mas tumpak na katumpakan hangga't maaari.
Mayroon kaming mahigpit na mga panuntunan sa pag-uukulan at nag-uugnay lamang sa mga kagalang-galang na mga site ng media, mga institusyong pang-akademikong pananaliksik at, hangga't maaari, ang mga pag-aaral ng medikal na pag-aaral. Tandaan na ang mga numero sa panaklong ([1], [2], atbp) ay maaaring i-click na mga link sa mga pag-aaral na ito.
Kung sa tingin mo na ang alinman sa aming nilalaman ay hindi tumpak, hindi napapanahon, o kung hindi pinag-uusapan, mangyaring piliin ito at pindutin ang Ctrl + Enter.
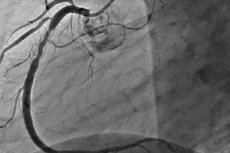
Ang restenosis ay ang pagbuo ng isang paulit-ulit na pagpapaliit ng 50% o higit pa sa lugar ng percutaneous coronary intervention. Ang restenosis ay kadalasang sinasamahan ng paulit-ulit na angina, na kadalasang nangangailangan ng paulit-ulit na interbensyon. Habang umuunlad ang PCI, bumaba ang insidente ng restenosis, at nagbago rin ang kalikasan nito.
Restenosis pagkatapos ng transluminal balloon coronary angioplasty (TBCA)
Pagkatapos ng TBCA, ang rate ng restenosis sa unang 6 na buwan ay 30-40%. Ang pangunahing mekanismo ng pag-unlad nito ay ang lokal na negatibong remodeling ng sisidlan, na, sa esensya, ay isang nababanat na pagbagsak ng arterial lumen, na pinalawak ng lobo sa panahon ng pamamaraan. Ang pagbuo ng lokal na thrombus at paglago ng neointimal ay gumaganap din ng isang kamag-anak na papel. Mayroong clinical (type 2 diabetes mellitus, acute coronary syndrome (ACS), history of restenosis), angiographic (LAD lesion, small vessel diameter, chronic total occlusion (CTO), long lesion, degenerated venous bypass grafts) at procedural (malaking residual stenosis, maliit na pagtaas ng vessel diameter bilang resulta ng balloon inflation) na mga risk factor para sa restenosis. Sa kaso ng restenosis, ang isang paulit-ulit na interbensyon ay karaniwang ginagawa. Ang tagumpay ng paulit-ulit na TBCA sa lugar ng restenosis ay maihahambing sa unang pamamaraan. Gayunpaman, sa bawat kasunod na TBCA para sa restenosis, ang panganib ng paulit-ulit na restenosis ay tumataas nang malaki. Pagkatapos ng 3rd attempt, umabot ito sa 50-53%. Bilang karagdagan, sa bawat paulit-ulit na TBCA, ang pagbuo ng restenosis ay mas malinaw kaysa sa una. Ang mga salik ng panganib para sa restenosis pagkatapos ng pangalawang TBCA para sa restenosis ay ang maagang paglitaw ng unang restenosis (60-90 araw pagkatapos ng procedure), pinsala sa LAD, pinsala sa multivessel, type 2 diabetes mellitus, arterial hypertension, hindi matatag na angina, at maraming balloon inflations sa unang pamamaraan. Dahil sa mataas na dalas ng restenosis at ang mekanismo ng pag-unlad nito, ang mga coronary stent ay ipinakilala sa klinikal na kasanayan, na ayon sa teorya ay dapat na tinanggal ang negatibong pag-aayos ng daluyan pagkatapos ng TBCA.
Ang mga unang pag-aaral na nagpakita ng bisa ng stenting ay ang STRESS at BENESTENT na pag-aaral na inilathala noong 1993. Kasama sa BENESTENT ang 516 na pasyente na may bagong diagnosed na stenosis sa coronary arteries na higit sa 3 mm ang lapad, na randomized sa dalawang grupo: conventional TBCA (n = 257) at TBCA na may stent placement (n). Pagkatapos ng 3 taon, ang rate ng restenosis sa panahon ng angiography ay 32% sa conventional TBCA group at 22% sa stenting group. Ang kamag-anak na pagbawas sa rate ng restenosis ay 31% (p <0.01). Ang stenting group ay nagkaroon din ng mas mababang pangangailangan para sa paulit-ulit na myocardial revascularization (10 kumpara sa 20.6% sa conventional TBCA group; p <0.01), na nauugnay sa isang mas mababang rate ng angina recurrence sa stenting group.
Ayon sa STRESS study (n = 407), ang rate ng restenosis ay mas mababa din sa stenting group (n ~ 205) kaysa sa conventional PTCA group (n = 202) - 31.6 vs. 42.1% (p <0.01). Ang bentahe ng paggamit ng mga stent kaysa sa conventional angioplasty sa kaso ng restenosis sa PTCA site ay ipinakita sa REST study, kung saan 383 mga pasyente na may restenosis ay randomized sa stenting o ulitin ang percutaneous transluminal coronary angioplasty. Ang angiographically detected repeat restenosis ay 18% na mas mababa sa stenting group (18 vs. 5.32%; p <0.03). Ang paulit-ulit na myocardial revascularization, na isang tagapagpahiwatig ng klinikal na makabuluhang restenosis, ay kinakailangan din ng mas kaunting madalas sa pangkat ng mga pasyente na sumailalim sa stenting (10 kumpara sa 27%; p <0.001). Kaya, ang mas mahusay na mga resulta sa paggamit ng stenting ay napatunayan hindi lamang sa mga katutubong arterya, kundi pati na rin sa kaso ng interbensyon para sa restenosis na nabuo pagkatapos ng TBCA.
Restenosis pagkatapos ng bare stent implantation (BSI)
Bagama't ang mga natuklasang coronary stent ay nagbawas ng saklaw ng restenosis ng 30-40% kumpara sa TBCA, 17-32% ng mga pasyente ang nagkakaroon ng in-stent restenosis kahit na pagkatapos ng stenting, na nangangailangan ng paulit-ulit na revascularization. Ang mekanismo ng pagbuo ng in-stent stenosis (ISS) ay naiiba sa na sa TBCA. Pagkatapos ng stenting, ang pangunahing kontribusyon sa restenosis ay neointima formation, sa halip na negatibong remodeling, tulad ng sa TBCA, na halos wala sa stent implantation site. Ang Neointima ay nabuo sa pamamagitan ng paglipat at paglaganap ng makinis na mga selula ng kalamnan na gumagawa ng extracellular matrix, na kasama ng mga selula ay bumubuo sa neointima. Bilang karagdagan, ang pagtitiyaga ng thrombus sa site ng stenting ay mahalaga din sa mga pasyente na may diabetes.
Ang pangunahing pag-uuri ng in-stent stenosis (ISS) ay ang pag-uuri na iminungkahi ng Mehrаn, na kinabibilangan ng apat na uri depende sa lawak at kalubhaan ng sugat: I type ang ISS - local (< 10 mm ang haba), II type - diffuse (> 10 mm ang haba), III type - proliferative (> 10 mm at umaabot sa lampas sa stent.ISS) at IV occlusion na humahantong sa uri ng stent. Ang unang uri ay nahahati sa mga subtype depende sa lokasyon sa stent: 1a - sa liko o sa pagitan ng mga stent, 1b - marginal, 1c - sa loob ng stent, 1d - multifocal.
Ang mga kadahilanan ng peligro para sa pagbuo ng VRS ay mga interbensyon sa venous bypass grafts, talamak na occlusion, ostial lesion, maliit na diameter ng vessel, pagkakaroon ng natitirang stenosis, stenting para sa VRS, maliit na post-procedural vessel diameter, LAD lesion, mahabang stent length, pagkakaroon ng diabetes, pagtatanim ng ilang stent sa isang sugat. May mga indikasyon ng impluwensya ng genetic factor, sa partikular na polymorphism ng glycoprotein IIIa gene at mutations ng methylenetetrahydrofolate reductase gene - ang gene encoding interleukin-1. Sa kaso ng pag-unlad ng marginal stent restenosis, ang pangunahing kadahilanan ng panganib ay isang binibigkas na atherosclerotic lesion sa stented segment.
Ang restenosis ay kadalasang nangyayari sa unang 6-8 na buwan pagkatapos ng percutaneous coronary intervention. Karamihan sa mga pasyente ay nagkakaroon ng mga klinikal na sintomas sa halos parehong oras. Ang VRS ay kadalasang ipinakikita ng paulit-ulit na angina. Ang hindi matatag na angina ay nangyayari nang hindi gaanong madalas (11-41% ng mga kaso). Nabubuo ang AMI sa 1-6% ng mga pasyente. Kaya, ang pinakakaraniwang sanhi ng angina sa panahon ng 1-6 na buwan pagkatapos ng stenting ay ang pagbuo ng VRS, na, bilang panuntunan, ay nangangailangan ng paulit-ulit na revascularization. Mayroong ilang mga paraan para sa paggamot sa VRS. Maaaring maisagawa ang maginoo na TBCA, na humahantong sa karagdagang pagpapalawak ng stent (56% na kontribusyon sa huling pagtaas ng diameter ng sisidlan) at itinutulak ang neointima sa pamamagitan ng mga stent cell (44% na kontribusyon sa huling pagtaas ng diameter). Gayunpaman, ang natitirang restenosis ay sinusunod sa karamihan ng mga kaso sa site ng interbensyon (sa average na 18%). Bilang karagdagan, pagkatapos ng TBCA, kinakailangan ang paulit-ulit na revascularization sa 11% ng mga kaso, mas madalas sa mga pasyente na may sakit na multivessel, mababang LVEF, sa kaso ng mga interbensyon sa venous bypass grafts o maagang paglitaw ng unang VRS. Ang panganib na magkaroon ng paulit-ulit na VRS pagkatapos ng TBCA ay depende rin sa uri ng lesyon at mula 10% sa kaso ng lokal na restenosis hanggang 80% sa kaso ng intra-stent occlusion. Ang pagtatanim ng LES sa site ng VRS ay hindi binabawasan ang panganib ng pag-ulit nito kumpara sa TBCA lamang.
Ang pangalawang paraan ng paggamot sa VRS ay brachytherapy, na kinabibilangan ng pagpasok ng radioactive source sa lumen ng coronary artery, na pumipigil sa paglaganap ng makinis na mga selula ng kalamnan at, nang naaayon, binabawasan ang panganib ng restenosis. Gayunpaman, ang mataas na halaga ng kagamitan, ang teknikal na pagiging kumplikado ng pamamaraan, at ang pagtaas ng saklaw ng late stent thrombosis (LT) ay halos ganap na hindi kasama ang brachytherapy mula sa klinikal na paggamit.
Ang isang rebolusyonaryong sandali sa paggamot sa VRS ay ang pagpapakilala ng mga stent na nagpapalabas ng droga. Kung ikukumpara sa LES sa mga katutubong arterya, binabawasan nila ang panganib ng VRS ng 70-80%. Ang unang data sa pagiging epektibo ng DES sa mga pasyente na may binuo na VRS ay nakuha sa TAXUS III registry ng mga pasyente, kung saan, kapag gumagamit ng SPG1 sa naturang mga pasyente, ang dalas ng pag-ulit ng VRS ay 16% lamang pagkatapos ng 6 na buwan, na mas mababa kaysa sa naunang nabanggit na mga pag-aaral sa TBCA. Sa TRUE registry, na kinabibilangan ng mga pasyente pagkatapos ng SES implantation para sa LES restenosis, pagkatapos ng 9 na buwan, ang paulit-ulit na revascularization ay kinakailangan sa mas mababa sa 5% ng mga pasyente, pangunahin na may diabetes mellitus at ACS. Inihambing ng TROPICAL na pag-aaral ang dalas ng paulit-ulit na restenosis sa mga pasyente pagkatapos ng pagtatanim ng DES sa site ng restenosis sa data ng mga pag-aaral ng GAMMA I at GAMMA II, kung saan ginamit ang brachytherapy bilang paraan ng paggamot. Pagkatapos ng 6 na buwan, Ang saklaw ng paulit-ulit na restenosis ay makabuluhang mas mababa sa pangkat ng SPS (9.7 vs 40.3%; p <0.0001). Mahalagang tandaan na ang saklaw ng stent thrombosis at myocardial infarction ay mas mababa din sa pangkat ng SPS (TS 0.6 vs 3.9%; p = 0.08; MI - 1.8 vs 9.4%; p = 0.004). Ang bentahe ng SPS sa brachytherapy ay nakumpirma sa randomized na pag-aaral ng SISR, kung saan 384 mga pasyente na may binuo VRS sa NSC ay randomized sa brachytherapy o SPS implantation group. Pagkatapos ng 9 na buwan, ang pangangailangan para sa paulit-ulit na revascularization ay mas mataas pagkatapos ng brachytherapy (19.2%) kaysa sa SPS implantation group (8.5%), na sumasalamin sa isang mas madalas na pag-ulit ng restenosis. Pagkatapos ng 3 taon, ang bentahe ng SPS sa mga tuntunin ng pagbabawas ng pangangailangan para sa paulit-ulit na revascularization dahil sa paulit-ulit na stent restenosis ay nanatili (19 vs 28.4%). Walang makabuluhang pagkakaiba sa saklaw ng trombosis sa pagitan ng mga grupo.
Ang pangunahing mga kadahilanan para sa pagbuo ng paulit-ulit na VRS sa mga pasyente na may LES sa kaso ng pagtatanim ng SPS ay isang maliit na diameter ng daluyan (<2.5 mm), nagkakalat na uri ng restenosis, at ang pagkakaroon ng talamak na pagkabigo sa bato na nangangailangan ng hemodialysis. Sa randomized na pag-aaral na TAXUS V ISR, nagpakita rin ang SPS ng mataas na kahusayan sa paggamot ng VRS, na binabawasan ang rate ng paulit-ulit na restenosis ng 54% kumpara sa brachytherapy.
Ang mga random na pagsubok na naghahambing sa bisa ng TBCA para sa VRS at DES implantation ay isinagawa din. Sa randomized na pagsubok ng RIBS-II, pagkatapos ng 9 na buwan, ang paulit-ulit na restenosis ay 72% na mas karaniwan pagkatapos ng pagtatanim ng DES kaysa pagkatapos ng TBCA, na nagbawas ng pangangailangan para sa paulit-ulit na revascularization mula 30 hanggang 11%. Inihambing ng pagsubok ng ISAR DESIRE ang bisa ng TBCA para sa VRS na may SPP o SPS implantation. Pagkalipas ng 6 na buwan, lumabas na ang parehong DES ay mas epektibo sa pagpigil sa paulit-ulit na restenosis kaysa sa TBCA (ang saklaw nito ay 44.6% kasama ang TBCA, 14.3% sa pangkat ng SPS, at 21.7% sa pangkat ng SPS), na nabawasan ang pangangailangan para sa paulit-ulit na revascularization. Sa isang direktang paghahambing ng SPP at SPS, natagpuan na ang SPS ay nabawasan ang pangangailangan para sa paulit-ulit na revascularization nang mas epektibo kaysa sa SPP (8 kumpara sa 19%). Kaya, binabawasan ng DES implantation ang saklaw ng paulit-ulit na LES VRS kumpara sa parehong TBCA at brachytherapy, na binabawasan ang bilang ng mga paulit-ulit na PCI at samakatuwid ay ginagawa ang kanilang implantasyon na pamamaraan ng pagpili sa mga naturang pasyente.
Restenosis pagkatapos ng pagtatanim ng drug-eluting stent (DES).
Sa kabila ng 70-80% na pagbaba sa saklaw ng in-stent stenosis kapag gumagamit ng DES kumpara sa LES, hindi nila ganap na maibukod ang pagbuo ng iatrogenic na kinahinatnan ng stenting. Ang kabuuang saklaw nito ay nananatiling nasa average na mas mababa sa 10%. Bilang karagdagan sa dami ng pagbaba sa saklaw ng restenosis, makabuluhang binago din nila ang uri ng restenosis na nangyayari. Kaya, pagkatapos ng pagtatanim ng DES, ang restenosis ay karaniwang nakatutok. Sa klinikal na paraan, tulad ng sa kaso ng LES, madalas itong nagpapakita ng sarili bilang isang pagbabalik ng matatag na angina (77%), mas madalas (8%) ito ay asymptomatic. Sa 5% ng mga kaso, ito ay nagpapakita ng sarili bilang hindi matatag na angina, at sa 10%, ang unang sintomas nito ay non-Q-wave myocardial infarction. Ang pangunahing mga kadahilanan sa pag-unlad ng DES restenosis ay type 2 diabetes mellitus, maliit na diameter ng daluyan, at ang lawak ng sugat. Walang malinaw na rekomendasyon para sa pamamahala ng mga naturang pasyente. Ang mga alternatibong opsyon ay ang muling pagtatanim ng isang DES (ng parehong uri o ibang isa), TBCA, o brachytherapy. Ang average na rate ng muling restenosis na may pangalawang DES ay 24%, at ito ay pareho kung ang parehong uri ng DES ay itinanim o iba.


 [
[